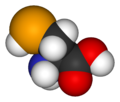
Selenocistein
| |||
| Nazivi | |||
|---|---|---|---|
| IUPAC naziv 3-Selanil-2-aminopropanska kiselina | |||
| Drugi nazivi L-Selenocistein; 3-Selanil-L-alanin; Selen cistein | |||
| Identifikacija | |||
| |||
3D model (Jmol) |
| ||
| ChEBI |
| ||
| ChemSpider |
| ||
| DrugBank |
| ||
| ECHA InfoCard | 100.236.386 | ||
| KEGG[2] |
| ||
| |||
SMILES
| |||
| Svojstva | |||
| C3H7NO2Se | |||
| Molarna masa | 168,07 g·mol−1 | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |||
 Y verifikuj (šta je Y verifikuj (šta je  Y Y Н ?) Н ?) | |||
| Reference infokutije | |||
Selenocistein (Se-Cys) je aminokiselina koja je prisutna u više enzima (na primer: glutationske peroksidaze, tetrajodotironin 5' dejodinaze, tioredoksin reduktaze, format dehidrogenaze, glicin reduktaze, i pojedine hidrogenaze).
Nomenklatura
IUPAC/IUBMB su zvanično preporučili simbole Sec i U za selenocistein.[5]
Struktura
Selenocistein je strukturno sličan sa cisteinom. Jedan atom selena zauzima mesto sumpora, formirajući selenol grupu. Proteini koji sadrže jedan ili više selenocisteinskih ostataka se nazivaju selenoproteinima.
Biologija
Selenocistein ima nižu pKa vrednost (5.47) i viši redukcioni potencijal od cisteina. Te osobine ga čine veoma podobnim za proteine koji učestvuju u antioksidantskim aktivnostima.[6]
Reference
- ^ Susan Budavari, ур. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th изд.). Merck Publishing. ISBN 0911910131.
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003. уреди
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature (JCBN) and Nomenclature Committee of IUBMB (NC-IUBMB) (1999). „Newsletter 1999”. European Journal of Biochemistry. 264 (2): 607—609. doi:10.1046/j.1432-1327.1999.news99.x. Архивирано из оригинала (reprint, with permission) 09. 06. 2011. г. Приступљено 06. 01. 2012.
- ^ BJ. Byun & YK. Kang (2011). „Conformational preferences and pK(a) value of selenocysteine residue.”. Biopolymers. 95 (5): 345—53. PMID 21213257. doi:10.1002/bip.21581.
Literatura
- F. Zinoni, A. Birkmann, T. C. Stadtman and A. Bock (1986). „Nucleotide sequence and expression of the selenocysteine-containing polypeptide of formate dehydrogenase (formate-hydrogen-lyase-linked) from Escherichia coli”. PNAS. 83 (13): 4650—4654. PMC 323799
 . PMID 2941757. doi:10.1073/pnas.83.13.4650. CS1 одржавање: Вишеструка имена: списак аутора (веза)
. PMID 2941757. doi:10.1073/pnas.83.13.4650. CS1 одржавање: Вишеструка имена: списак аутора (веза) - F. Zinoni, A. Birkmann, W. Leinfelder and A. Bock (1987). „Cotranslational insertion of selenocysteine into formate dehydrogenase from Escherichia coli directed by a UGA codon”. PNAS. 84 (10): 3156—3160. PMC 304827
 . PMID 3033637. doi:10.1073/pnas.84.10.3156. CS1 одржавање: Вишеструка имена: списак аутора (веза)
. PMID 3033637. doi:10.1073/pnas.84.10.3156. CS1 одржавање: Вишеструка имена: списак аутора (веза) - Boyce E. Cone; Rafael Martin Del Rio; Joe Nathan Davis & Thressa C. Stadtman (1976). „Chemical characterization of the selenoprotein component of clostridial glycine reductase: identification of selenocysteine as the organoselenium moiety”. PNAS. 73 (8): 2659—63. PMC 430707
 . PMID 1066676. doi:10.1073/pnas.73.8.2659.
. PMID 1066676. doi:10.1073/pnas.73.8.2659.
Spoljašnje veze
- p
- r
- u